ОбЙИарЄСе ЕЭЙЗеш 5 ОбЙИатЄрЧрХЙЕь (Covalent bonds)
ОбЙИатЄрЧрХЙЕь (Covalent bond)
рЛчЙЁвУЪУщвЇОбЙИаУаЫЧшвЇЭаЕЭСЂЭЇЭтХЫаЁбКЭтХЫа (УЧСЗбщЇИвЕи Be ЋжшЇрЛчЙтХЫа) ИвЕиЗешрЛчЙЭтХЫаЙбщЙЪшЧЙуЫшСерЧрХЙЋьЭдрХчЁЕУЭЙЕбщЇсЕш
4 ЂжщЙфЛ ЄзЭЄвУьКЭЙ ( C ) сЕшИвЕиЗешСерЧрХЙЋьЭдрХчЁЕУЭЙрЗшвЁбК 4 ЭеЁ 2 ИвЕи ЄзЭ Sn ЁбК
Pb рЛчЙтХЫа
ЙЭЁЈвЁЙбщЙТбЇСеЭтХЫаЭеЁЊЙдДЫЙжшЇЗешСерЧрХЙЋьЭдрХчЁЕУЭЙрЗшвЁбК 1
ЄзЭфЮтДУрЈЙ ( H ) тДТЗбшЧфЛсХщЧЭтХЫарЛчЙИвЕиЗешСеЄшвЭдрХчЁтЕУрЙЁвЕдЧдЕе (EN) сХаОХбЇЇвЙфЭЭЭфЙрЋЊбЙ (IE) ЪйЇ ЗгуЫщрЪеТЭдрХчЁЕУЭЙТвЁ
ЈжЇфСшЪвСвУЖуЫщЫУзЭУбКЭдрХчЁЕУЭЙЁбЙЭТшвЇЪСКйУГь фСшрЫСзЭЙЁУГеЂЭЇЁвУЪУщвЇОбЙИафЭЭЭЙдЁ ЭаЕЭСЂЭЇЭтХЫаЗешрЧрХЙЋьЭдрХчЁЕУЭЙТбЇфСшрЛчЙфЛЕвСЁЎЭЭЁрЕчЕЈаСеЭдрХчЁЕУЭЙрДешТЧЭТйшуЙКвЇЭЭУьКдЗбХ ЈауЊщЧдИеЙгЭдрХчЁЕУЭЙрДешТЧЗешЕшвЇНшвТЕшвЇЁчСеЭТйшСвуЊщУшЧСЁбЙрЛчЙЄйш
ц рЁдДЁвУЋщЭЙЗбК (overlap) ЂЭЇЭЭУьКдЗбХЋжшЇЁбЙсХаЁбЙ ЖщвЋщЭЙЗбКЁбЙЗешЪшЧЙЛХвТЂЭЇЭЭУьКдЗбХрУеТЁЧшвЋдЁСвКЭЙ
( sigma bond ,) ЖщвЋщЭЙЗбКЁбЙЗвЇДщвЙЂщвЇрУеТЁЧшвфОКЭЙДь
( pi bond ,bonb) ДбЇУйЛ
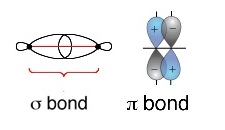
ЁвУуЊщЭдрХчЁЕУЭЙУшЧСЁбЙЙещрЛчЙфЛрОзшЭЗгуЫщЗбщЇ 2
НшвТСерЧрХЙЋьЭдрХчЁЕУЭЙрЛчЙфЛЕвСЁЎЭЭЁрЕчЕЄзЭЄУК 8 сЕшСеЂщЭТЁрЧщЙЭТйшКщвЇуЙКвЇЁУГеЗешЭвЈЈаЙщЭТЁЧшв 8
ЫУзЭСвЁЁЧшв 8 фДщ
сХаЁвУуЊщЭдрХчЁЕУЭЙУшЧСЁбЙрЛчЙЄйш ц
ДбЇЁХшвЧСвЙещрУеТЁЧшврЛчЙЁвУЪУщвЇОбЙИатЄрЧрХЙЕь ( Covalent bonding ) ЈаСефДщЕбщЇсЕш 1
ЖжЇ 3 Єйш сЕшХаЭаЕЭСЈауЊщЭдрХчЁЕУЭЙУшЧСЁбКЭаЕЭСЭзшЙЁешЄйш уЫщЪбЇрЁЕДйЧшвсЕшХаЭаЕЭСТбЇЂвДЭдрХчЁЕУЭЙЭеЁЁешЕбЧЈжЇЈаЄУК
8
ЫУзЭрЛчЙфЛЕвСЁЎЭЭЁрЕЕ (octet rule) ЭаЕЭСЁчЈауЊщрЧрХЙЋьЭдрХчЁЕУЭЙрЗшвЁбКЈгЙЧЙЗешТбЇЂвДУшЧСЁбКЭдрХчЁЕУЭЙЂЭЇЭаЕЭСЭзшЙ тДТЭвЈрЛчЙЭаЕЭСЂЭЇИвЕирДеТЧЁбЙЫУзЭрЛчЙИвЕиЕшвЇЊЙдДЁбЙЁчфДщ
уЙЁУГеЗешрЛчЙИвЕирДеТЧЁбЙЈафСшТишЇТвЁ рОУвасЕшХаЭаЕЭССеЁвУЈбДЭдрХчЁЕУЭЙрЫСзЭЙЁбЙ ЈгЙЧЙЭдрХчЁЕУЭЙЗешсЕшХаЭаЕЭСЂвДфЛЈжЇрЗшвЁбЙ рЊшЙ Cl
O сХа N ЈаСерЧрХЙЋьЭдрХчЁЕУЭЙДбЇЙещ
 Cl ЗиЁЭаЕЭССерЧрХЙЋьЭдрХчЁЕУЭЙ = 7 ЂвДЭеЁ 1
ЭдрХчЁЕУЭЙЈаЄУК 8 Жщв
Cl 2 ЭаЕЭС
ЭТйшУшЧСЁбЙ
сЕшХаЭаЕЭСЈауЊщрЧрХЙЋьЭдрХчЁЕУЭЙ
1 ЕбЧ УшЧСЁбКЭеЁЭаЕЭСЫЙжшЇ ЈжЇрЛчЙЁвУуЊщЭдрХчЁЕУЭЙУшЧСЁбЙ 1 Єйш рУеТЁЧшвОбЙИарДешТЧ (single bond)
ДбЇУйЛ Cl ЗиЁЭаЕЭССерЧрХЙЋьЭдрХчЁЕУЭЙ = 7 ЂвДЭеЁ 1
ЭдрХчЁЕУЭЙЈаЄУК 8 Жщв
Cl 2 ЭаЕЭС
ЭТйшУшЧСЁбЙ
сЕшХаЭаЕЭСЈауЊщрЧрХЙЋьЭдрХчЁЕУЭЙ
1 ЕбЧ УшЧСЁбКЭеЁЭаЕЭСЫЙжшЇ ЈжЇрЛчЙЁвУуЊщЭдрХчЁЕУЭЙУшЧСЁбЙ 1 Єйш рУеТЁЧшвОбЙИарДешТЧ (single bond)
ДбЇУйЛ

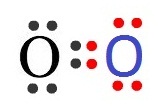
ЭЭЁЋдрЈЙ (O) ЗиЁЭаЕЭССерЧрХЙЋьЭдрХчЁЕУЭЙ = 6 ЂвДЭеЁ 2 ЭдрХчЁЕУЭЙЈаЄУК 8 ЖщвЭЭЁЋдрЈЙ 2
ЭаЕЭС ЭТйшУшЧСЁбЙ сЕшХаЭаЕЭСЈауЊщрЧрХЙЋьЭдрХчЁЕУЭЙ 2
ЕбЧ УшЧСЁбКЭеЁЭаЕЭСЫЙжшЇ ЈжЇрЛчЙЁвУуЊщЭдрХчЁЕУЭЙУшЧСЁбЙ 2 Єйш рУеТЧшвОбЙИаЄйш (double bond ) ДбЇУйЛ
фЙтЕУрЈЙ (N) ЗиЁЭаЕЭССерЧрХЙЋьЭдрХчЁЕУЭЙ = 5 ЂвДЭеЁ 3 ЭдрХчЁЕУЭЙЈаЄУК 8 ЖщвфЙтЕУрЈЙ 2
ЭаЕЭС ЭТйшУшЧСЁбЙ сЕшХаЭаЕЭСЈауЊщрЧрХЙЋьЭдрХчЁЕУЭЙ 3
ЕбЧ УшЧСЁбКЭеЁЭаЕЭСЫЙжшЇ ЈжЇрЛчЙЁвУуЊщЭдрХчЁЕУЭЙУшЧСЁбЙ 3 Єйш рУеТЁЧшвОбЙИаЪвС
(triple bond) ДбЇУйЛ

сЕшЖщврЛчЙЭаЕЭСЂЭЇИвЕиЕшвЇЊЙдДЁбЙЋжшЇЭвЈСерЧрХЙЋьЭдрХчЁЕУЭЙрЗшвЁбЙЫУзЭфСшрЗшвЁбЙЁчфДщ ЁвУОдЈвУГвЧшвЈа.уЊщЭдрХчЁЕУЭЙУшЧСЁбЙЁешЄйшЈаСеЄЧвСТишЇТвЁЂжщЙ рЊшЙ
ЁУГе Cl ЁбК
O
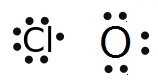
Cl ТбЇЂвДЭдрХчЁЕУЭЙЭеЁ 1
ЕбЧЈжЇЈаЄУК 8 ЈжЇуЊщрЧрХЙЋьЭдрХчЁЕУЭЙрОеТЇ 1
ЕбЧУшЧСЁбК O
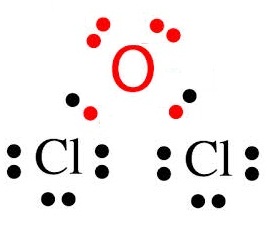
O ТбЇЂвДЭдрХчЁЕУЭЙЭеЁ 2 ЕбЧЈжЇЈаЄУК
8 ЈжЇЕщЭЇуЊщрЧрХЙЋьЭдрХчЁЕУЭЙ 2 ЕбЧУшЧСЁбК Cl
ЁУГеЙещЈжЇЕщЭЇуЊщ Cl ЈгЙЧЙ 2
ЭаЕЭС сЕшуЊщ O рОеТЇ
1 ЭаЕЭС ДбЇУйЛ
ЖщврЛчЙЭаЕЭСЂЭЇ Cl ЁбК
N ЈарЛчЙДбЇЙещ

Cl ТбЇЂвДЭдрХчЁЕУЭЙЭеЁ 1
ЕбЧЈжЇЈаЄУК 8 ЈжЇуЊщрЧрХЙЋьЭдрХчЁЕУЭЙрОеТЇ 1
ЕбЧУшЧСЁбК N
N ТбЇЂвДЭдрХчЁЕУЭЙЭеЁ 3 ЕбЧЈжЇЈаЄУК 8 ЈжЇЕщЭЇуЊщрЧрХЙЋьЭдрХчЁЕУЭЙ 3 ЕбЧУшЧСЁбК Cl
ЁУГеЙещЈжЇЕщЭЇуЊщ Cl ЈгЙЧЙ 3 ЭаЕЭС
сЕшуЊщ N рОеТЇ
1 ЭаЕЭС ДбЇУйЛ
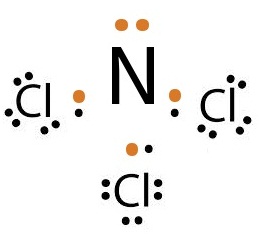
ЖщврЛчЙЭаЕЭСЂЭЇ N ЁбК
O ЈарЛчЙДбЇЙещ

N ТбЇЂвДЭдрХчЁЕУЭЙЭеЁ
3 ЕбЧЈжЇЈаЄУК 8 ЈжЇЕщЭЇуЊщрЧрХЙЋьЭдрХчЁЕУЭЙ 3 ЕбЧУшЧСЁбК O
O ТбЇЂвДЭдрХчЁЕУЭЙЭеЁ
2 ЕбЧЈжЇЈаЄУК
8 ЈжЇЕщЭЇуЊщрЧрХЙЋьЭдрХчЁЕУЭЙ 2 ЕбЧУшЧСЁбК N
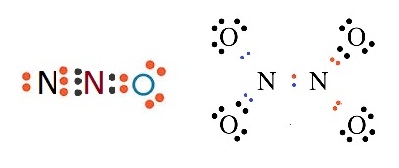
ЁУГеЙещЁвУЪУщвЇОбЙИарЛчЙфЛфДщЫХвТсКК
ЈжЇСеЪвУЛУаЁЭКЫХвТЊЙдД рЊшЙ N2O N2O4 ДбЇУйЛ
ЁвУуЊщЭдрХчЁЕУЭЙУшЧСЁбЙрЛчЙЄйш ц ДбЇЁХшвЧЙещЈаСеЕбщЇсЕш 1 ЖжЇ 3
Єйш
- ЖщвуЊщЭдрХчЁЕУЭЙУшЧСЁбЙ 1 ЄйшрУеТЁЧшв ОбЙИарДешТЧ (single bond)
- ЖщвуЊщЭдрХчЁЕУЭЙУшЧСЁбЙ 2 ЄйшрУеТЁЧшв ОбЙИаЄйш (double
bond)
- ЖщвуЊщЭдрХчЁЕУЭЙУшЧСЁбЙ 3 ЄйшрУеТЁЧшв ОбЙИаЪвС (triple
bond)
ЁвУЗешЭаЕЭСЈауЊщЭдрХчЁЕУЭЙУшЧСЁбЙЁешЄйшЙбщЙрЛчЙфЛЕвСЄЧвСрЫСваЪСЧшв
ЈауЊщУшЧСЁбЙЭТшвЇфУЈжЇЈаЗгуЫщсЕшХаЭаЕЭССерЧрХЙЋьЭдрХчЁЕУЭЙрЛчЙфЛЕвСЁЎЭЭЁрЕчЕ (сЕшСеЁУГеТЁрЧщЙЭТйшКщвЇ)
(ЄХдщЁ ЊСЁвУЪУщвЇОбЙИатЄрЧрХЙЕьУаЫЧшвЇ F ЁбК F
сХа H ЁбК F)
(ЄХдщЁ ЊСЁвУЪУщвЇЁбЙИатЄрЧрХЕьУаЫЧшвЇ H-H , O=O сХа H-O )
ОбЙИарДешТЧ (single bond)
СеЭаЕЭСЂЭЇИвЕирЛчЙЈгЙЧЙСвЁЗешЭТйшУЧСЁбКЭаЕЭСЭзшЙДщЧТЁвУуЊщЭдрХчЁЕУЭЙУшЧСЁбЙ 1
Єйш рЛчЙЁвУЪУщвЇОбЙИарДешТЧ рЊшЙ H2 F2 Cl2 Br2 I2
HF HCl HBr HI
H2S CH4 …. ЈарЫчЙфДщЧшвЁвУЪУщвЇОбЙИаЪвСвУЖрЁдДЂжщЙЁбКЭаЕЭСЂЭЇИвЕирДеТЧЁбЙ ЫУзЭрЁдДЂжщЙЁбКЭаЕЭСЂЭЇИвЕиЕшвЇЊЙдДЁбЙЁчфДщ тДТЗбшЧфЛЈаОКЧшвЭаЕЭСЗешСерЧрХЙЋьЭдрХчЁЕУЭЙ
= 7
ЈаЪУщвЇОбЙИарДешТЧрЪСЭ фДщсЁш F
Cl Br сХа
I УЧСЗбщЇ H ЋжшЇСерЧрХЙЋьЭдрХчЁЕУЭЙ = 1 ЁчЈаЪУщвЇОбЙИарДешТЧрЊшЙЁбЙ ОдЈвУГвЭаЕЭСЂЭЇ Cl
СеЁвУЈбДЭдрХчЁЕУЭЙДбЇЙещ ;
17Cl 2 8 7

рСзшЭЭаЕЭСЂЭЇ Cl ЈгЙЧЙ 2 ЭаЕЭСЪУщвЇОбЙИаЁбЙ
сЕшХаЭаЕЭСЁчЈаЙгЭдрХчЁЕУЭЙрДешТЧуЙЭЭУьКдЗбХ 3p
СвуЊщУшЧСЁбЙтДТЋщЭЙЗбК (overlap) ДбЇУйЛ

ЁвУЋщЭЙЗбКЂЭЇЭЭУьКдЗбХрЛчЙХбЁЩГаЂЭЇЋдЁСв КЭЙДь
ДбЇУйЛ
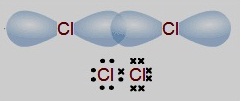
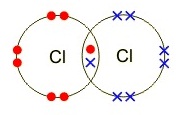
ЁвУЗешЄХЭУеЙ 2 ЭаЕЭСуЊщЭдрХчЁЕУЭЙУшЧСЁбЙ
1 Єйш СеМХуЫщЄХЭУеЙЗбщЇ 2
ЭаЕЭСрЁдДсУЇДжЇДйДЁбКЭдрХчЁЕУЭЙЄйшрДеТЧЁбЙ ЈжЇЗгуЫщЄХЭУеЙЗбщЇ 2
ЭаЕЭСЙещУЧСЕбЧЁбЙрЛчЙтСрХЁиХЂЭЇЄХЭУеЙ (Cl2) ЁгЫЙДуЫщрУеТЁЭдрХчЁЕУЭЙЄйшЗешуЊщУшЧСЁбЙЧшвЭдрХчЁЕУЭЙЄйшУшЧСОбЙИа
(Share pair
electron ; Bond pair electron) ЁУГеЙещрЛчЙОбЙИарДешТЧрОУвауЊщЭдрХчЁЕУЭЙУшЧСЁбЙ
1 Єйш ЪгЫУбКЭдрХчЁЕУЭЙЗешфСшфДщуЊщУшЧСЁбЙЂЭЇЗбщЇ 2
ЭаЕЭСрУеТЁЧшвЭдрХчЁЕУЭЙЄйштДДрДешТЧ (unshared pair electron ; lone pair electron) ЙбКрЉОварЧрХЙЋьЭдрХчЁЕУЭЙрЗшвЙбщЙ (Се 6 Єйш )
рУвЪвСвУЖрЂеТЙсЪДЇЁвУЪУщвЇОбЙИатЄрЧрХЙЕьДщЧТЪйЕУХдЧЭдЪ тДТуЊщЈиД 1
ЈиДсЗЙЭдрХчЁЕУЭЙ 1 ЕбЧ сЕшуЫщсЪДЇрЉОварЧрХЙЋьЭдрХчЁЕУЭЙрЗшвЙбщЙ ЫУзЭрЂеТЙТшЭтДТуЊщрЪщЙ 1
рЪщЙ
сЗЙЭдрХчЁЕУЭЙЄйшУшЧСОбЙИа 1 ЄйшЁчфДщ
ДбЇУйЛ

УаТаЫшвЇУаЫЧшвЇЙдЧрЄХеТЪЂЭЇЭаЕЭСЗешЪУщвЇОбЙИарУеТЁЧшв ЄЧвСТвЧОбЙИа (Bond length) сХаЄУжшЇЫЙжшЇЂЭЇЄЧвСТвЧОбЙИаЄзЭ УбШСеЂЭЇЭаЕЭСЊЙдДУбШСетЄрЧрХЙЕь
(covalent radius) рЛчЙЁвУКЭЁЂЙвДЂЭЇЭаЕЭСЧдИеЫЙжшЇ ЂЙвДЭаЕЭСЗешрЛчЙУбШСетЄрЧрХЙЕь
ЈарХчЁЁЧшвЭаЕЭСЈУдЇрОУваСеЁвУрЫХзшЭСЋщЭЙЗбКЁбЙ ЂЙвДЈУдЇЂЭЇЭаЕЭСЗешфСшСеЁвУЋщЭЙЗбКЁбЙрУеТЁЧшвУбШСесЧЙрДЭУьЧвХЪь
(Van der Waals radius) ДбЇУйЛ
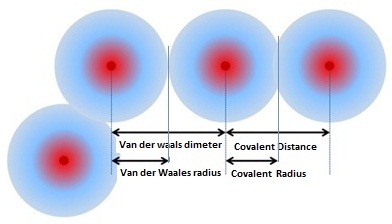
ОбЙИатЄЭЭУьДдрЙЕтЄрЧрХЙЕь
рЛчЙОбЙИатЄрЧрХЙЕьЊЙдДОбЙИарДешТЧ сЕшЕЁЕшвЇЈвЁОбЙИатЄрЧрХЙЕьИУУСДвЄзЭ ЭдрХчЁЕУЭЙЄйшУшЧСОбЙИарЛчЙЭдрХчЁЕУЭЙЂЭЇЭаЕЭСуДЭаЕЭСЫЙжшЇЗбщЇЄйш фСшфДщрЁдДЈвЁЗбщЇ 2
ЭаЕЭСЙгЭдрХчЁЕУЭЙЈгЙЧЙрЗшвЁбЙСвуЊщУшЧСЁбЙ
( A coordinate covalent bond is a covalent bond in
which both electrons of a shared pair come from one of the two atoms involved
in the bond'.) рЊшЙ NH4+ рЁдДЈвЁ NH3 ЋжшЇСеЭдрХчЁЕУЭЙЄйштДДрДешТЧЭТйш 1
Єйш ЪУщвЇОбЙИаЁбК H+ ЋжшЇфСшСеЭдрХчЁЕУЭЙрХТ ДбЇЪСЁвУсХаДбЇУйЛ
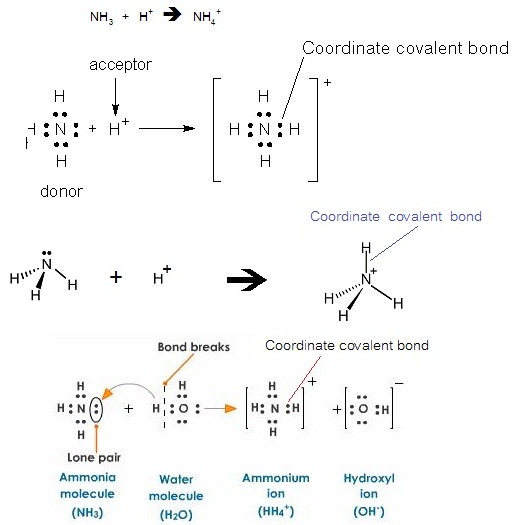
уЙЪвУХаХвТЂЭЇЁУДЊЙдДЕшвЇ ц ЁУДЈасЕЁЕбЧуЫщ H+
ЈвЁЙбщЙЈаУЧСЕбЧЁбК
H2O
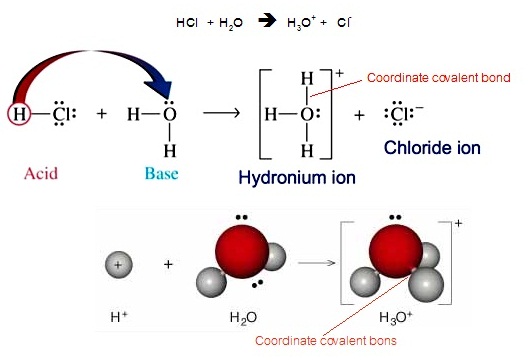
тДТрЁдДОбЙИатЄЭЭУьДдрЙЕтЄрЧрХЙЕьЁбКЭдрХчЁЕУЭЙЄйштДДрДешТЧЂЭЇ O ЁХвТрЛчЙ H3O+ ЫУзЭфЮтДУрЙеТСфЭЭЭЙ ДбЇЪСЁвУсХаДбЇУйЛ
SO3 рЁдДЈвЁ SO2 ЋжшЇСеЭдрХчЁЕУЭЙЄйштДДрДешТЧ 1
Єйш ЭТйшЗешЭаЕЭСЂЭЇ S ЈвЁЙбщЙ O ЭеЁ 1ЭаЕЭССвЪУщвЇОбЙИатДТуЊщЭдрХчЁЕУЭЙЄйштДДрДешТЧЙещ ДбЇУйЛ

- ЁвУЪУщвЇОбЙИауЙХбЁЩГаЙещрЛчЙЛЏдЁдУдТвУаЫЧшвЇЁУДЁбКрКЪЕвСЗФЩЎеЁУД
рКЪ ЂЭЇХдЧЭдЪ ЗешЁХшвЧЧшв ЁУДЄзЭЪвУЗешУбКЄйшЭдрХчЁЕУЭЙЈвЁЪвУЭзшЙ рКЪЄзЭЪвУЗешуЫщЄйшЭдрХчЁЕУЭЙсЁшЪвУЭзшЙ ДбЇУйЛ
**
тЭтЋЙ (O3) СеЁвУЪУщвЇОбЙИаДбЇУйЛ
ЈЇОдЈвУГвЧшвОбЙИатЄЭЭУьДдрЙЕтЄрЧрХЙЕьЭТйшЗешуД
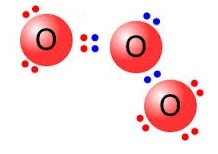
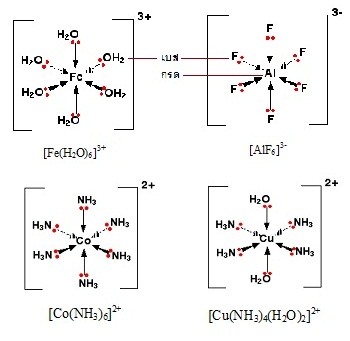
уЙЪвУЛУаЁЭКрЊдЇЋщЭЙ (complex compounds)
ЊЙдДЕшвЇ ц ХдсЁЙ (ligands) ЫУзЭЭЙиРвЄЗешХщЭСУЭКЭаЕЭСЁХвЇ ЈаЕщЭЇСеЭдрХчЁЕУЭЙЄйштДДрДешТЧЭТйшДщЧТЈжЇЈарЛчЙХдсЁЙДьфДщ
ЭЙиРвЄЗешфСшСеЭдрХчЁЕУЭЙЄйштДДрДешТЧЈарЛчЙХдсЁЙДьфСшфДщ рСзшЭХдсЁЙДьХщЭСУЭКЭаЕЭСЁХвЇ (central
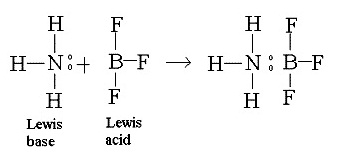
atom) ЈауЊщЭдрХчЁЕУЭЙЄйштДДрДешТЧДбЇЁХшвЧЪУщвЇОбЙИатЄЭЭУьДдрЙЕтЄрЧрХЙЕьЁбЙ ХдсЁЙДьЈжЇрЛчЙМйщуЫщЄйшЭдрХчЁЕУЭЙ (electron
donor) ЈжЇрЛчЙрКЪЕвСЗФЩЎеЂЭЇХдЧЭдЪ уЙЂГаЗешЭаЕЭСЁХвЇрЛчЙМйщУбКЄйшЭдрХчЁЕУЭЙ(
electron acceptor ) ЈжЇЁУДЕвСЗФЩЎеЂЭЇХдЧЭдЪ ДбЇУйЛ
ОбЙИаЄйш (double
bond)
СеЭаЕЭСЂЭЇИвЕиЭТйшрЛчЙЈгЙЧЙСвЁрЊшЙЁбЙЗешЭТйшУшЧСЁбКЭаЕЭСЭзшЙДщЧТЁвУЪУщвЇОбЙИаЄйш ЄзЭуЊщЭдрХчЁЕУЭЙУшЧСЁбКЭаЕЭСЭзшЙЈгЙЧЙ 2
Єйш ( 4 ЭдрХчЁЕУЭЙ) рЊшЙ O2 CO2 CS2 … ЁвУЪУщвЇОбЙИаЄйшЂЭЇЭаЕЭСуЙРвЧаЛЁЕдЈарЁдДЂжщЙЁбКЭаЕЭСЗешСерЧрХЙЋьЭдрХчЁЕУЭЙрЗшвЁбК 6
(ЂвДЭеЁ 2 ЭдрХчЁЕУЭЙЈаЄУК 8 ) ОдЈвУГвЁвУЈбДЭдрХчЁЕУЭЙЂЭЇЭЭЁЋдрЈЙ рЛчЙДбЇЙещ
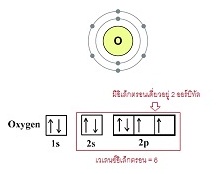
рСзшЭЭЭЁЋдрЈЙ 2 ЭаЕЭСЪУщвЇОбЙИаЁбЙ ЈауЊщЭдрХчЁЕУЭЙУшЧСЁбЙ 2
Єйш тДТЁвУЋщЭЙЗбК (overlap) УаЫЧшвЇЭЭУьКдЗбХЗешСеЭдрХчЁЕУЭЙрДешТЧЂЭЇсЕшХаЭаЕЭС ДбЇУйЛ
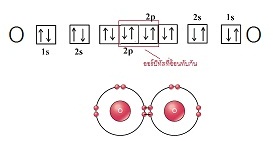
рЂеТЙсЪДЇДщЧТЪйЕУХдЧЭдЪДбЇЙещ
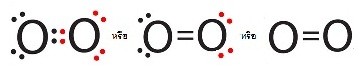
ЁвУЋщЭЙЗбКЂЭЇЭЭУьКдЗбХуЙтСрХЁиХЂЭЇ O2 Се
2 сКК ЄзЭ
ЋщЭЙЗбКЗешЪшЧЙЛХвТЂЭЇЭЭУьКдЗбХ (sigma
bond) сХаЋщЭЙЗбКЗвЇДщвЙЂщвЇ
(pi bond) ДбЇУйЛ
сЕшЭТшвЇфУЁчЕвСИвЕиКвЇИвЕиЪвСвУЖЪУщвЇОбЙИафДщЫХвТсККуЙрЧХврДеТЧЁбЙтДТЂжщЙЭТйшЁбКЊЙдДЂЭЇИвЕиЗешЈаЪУщвЇОбЙИаЁбЙ рЊшЙ CH2O
сХа CCl2O ОдЈвУГвЗеш C ОКЧшвЪУщвЇОбЙИаЄйшЁбК O ЈгЙЧЙ
1 ОбЙИа сЕшЪУщвЇОбЙИарДешТЧЭеЁ 2
ОбЙИаЁбК H ЈгЙЧЙ 2
ЭаЕЭС ЫУзЭ Cl 2
ЭаЕЭСЕвСХгДбК ДбЇУйЛ

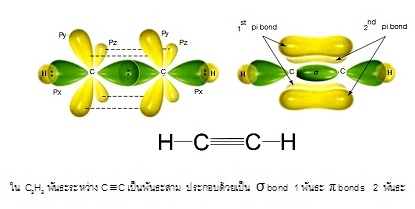
ОбЙИаЪвС (triple bond)
ЭаЕЭСуЙРвЧаЛЁЕдЗешЈаЪУщвЇОбЙИаЪвСЁбКЭаЕЭСЭзшЙЈаСерЧрХЙЋьЭдрХчЁЕУЭЙрЗшвЁбК 5 (ЂвДЭеЁ
3 ЈаЄУК 8) ОдЈвУГвЁвУЈбДЭдрХчЁЕУЭЙЂЭЇфЙтЕУрЈЙЈарЛчЙДбЇЙещ
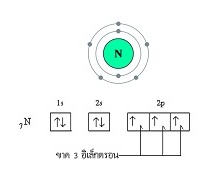
рСзшЭЭаЕЭСЂЭЇфЙтЕУрЈЙ 2
ЭаЕЭСЪУщвЇОбЙИаЁбЙ
ЈаЪУщвЇОбЙИаЁбЙтДТуЊщЭдрХчЁЕУЭЙУшЧСЁбЙ
3 Єйш рУеТЁЧшвОбЙИаЪвС (Triple
bond) ДбЇЙещ
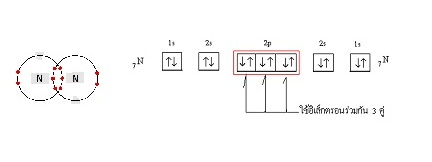
рЂеТЙсЪДЇДщЧТЪйЕУХдЧЭдЪДбЇЙещ

ОбЙИаЪвСЈаЛУаЁЭКДщЧТ sigma bond 1 ОбЙИаЁбК pi bond 2
ОбЙИа ДбЇУйЛ

(ЄХдщЁ ЊСЧеДеЗбШЙьсЪДЇЁвУрЁдД sigms bond сХа pi bond ЂЭЇ N2)
ЋдЁСвКЭЙДьЁбКфОКЭЙДь (Sigma and
pi bond)
ЁвУЪУщвЇОбЙИатЄрЧрХЙЕьСе
2 сКК ЄзЭ
ЋдЁСвКЭЙДь (σ
bond ) сХа фОКЭЙДь ( pi bond ,
π
bonds)
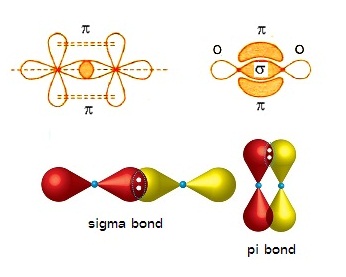
ЋдЁСвКЭЙДь (σ bond ) рЛчЙЁвУЋщЭЙЗбК(overlap)ЗешЪшЧЙЛХвТЂЭЇЭЭУьКдЗбХ
рЁдДЂжщЙЁбКЭЭУьКдЗбХЊЙдДрДеТЧЁбЙЫУзЭЕшвЇЊЙдДЁбЙЁчфДщ ЖщвОбЙИарЛчЙОбЙИарДешТЧЈарЛчЙЋдСвКЭЙДьрЪСЭ ДбЇУйЛ
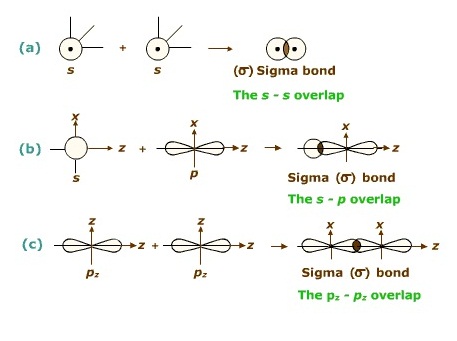
фОКЭЙДь ( pi bond , π bonds) ЄзЭЁвУЋщЭЙЗбК (overlap) ЁбЙКУдрЧГДщвЙЂщвЇЂЭЇЭЭУКдЗбХ фОКЭЙЈарЁдДЊжщЙуЙОбЙИаЄйшсХаОбЙИаЪвС фСшСеуЙОбЙИарДешТЧ ЖщврЛчЙОбЙИаЄйшЈаЛУаЁЭКДщЧТ σ bond 1 ОбЙИа π bonds 1 ОбЙИаЖщврЛчЙОбЙИаЪвСЈаЛУаЁЭКДщЧТ σ bond 1 ОбЙИа
π bonds 2
ОбЙИа ДбЇУйЛ
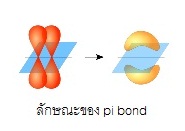
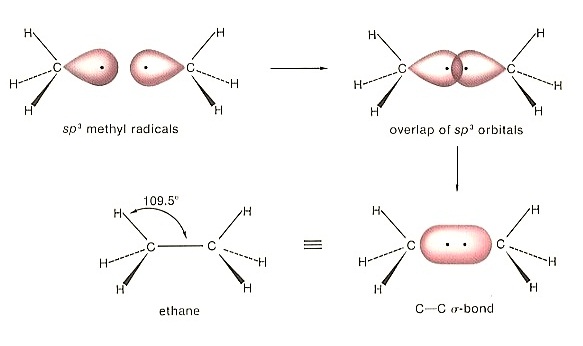
уЙ C2H6 ОбЙИаУаЫЧшвЇ C-C рЛчЙОбЙИарДешТЧ сХарЛчЙ σ bond

уЙ C2H4 ОбЙИаУаЫЧшвЇ C=C рЛчЙОбЙИаЄйш ЛУаЁЭКДщЧТрЛчЙ σ bond 1 ОбЙИа
π
bonds 1 ОбЙИа
ЁвУЁХшвЧЖжЇЋдЁСвКЭЙЁбКфОКЭЙЈаСеСвЁуЙрУзшЭЇЪвУЛУаЁЭКЂЭЇЄвУьКЭЙ
(рЄСеЭдЙЗУеТь , organic chemistry) ОбЙИаДбЇЁХшвЧЈарЁдДЂжщЙУаЫЧшвЇЭаЕЭСЂЭЇ C ЁбК C ЪбСОбЙИьЁбКЁвУрЁдДфЮКУдфДрЋЊбЙЂЭЇ C ЗешрЛчЙфЛфДщ
3 сКК ЄзЭ sp sp2 сХа sp3 ДбЇУйЛ
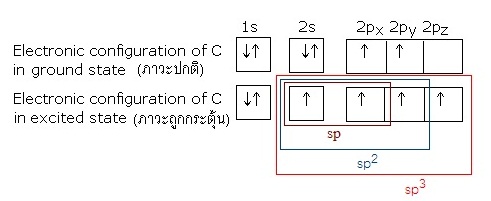
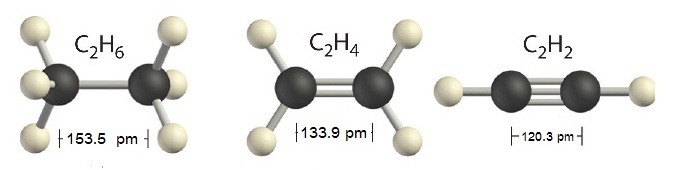
фЮКУдДЭЭУьКдЗбХ sp sp2 сХа sp3 СеУйЛЗУЇрУЂвЄГдЕрЛчЙ рЪщЙЕУЇ (linear) ЪвСрЫХешТСсКЙУвК (trigonal plana) сХаЗУЇрЫХешТСЪешЫЙщв (tetrahedral) ЕвСХгДбК
фЮКУдДЭЭУьКдЗбХ sp рЁдДЂжщЙЈвЁЁвУУЧСЕбЧУаЫЧшвЇ orbital
2s ЁбК orbital 2px фЮКУдДЭЭУьКдЗбХЗешрЁдДЂжщЙСеУйЛУшвЇрЛчЙрЪщЙЕУЇ
(Linear) ДбЇУйЛ
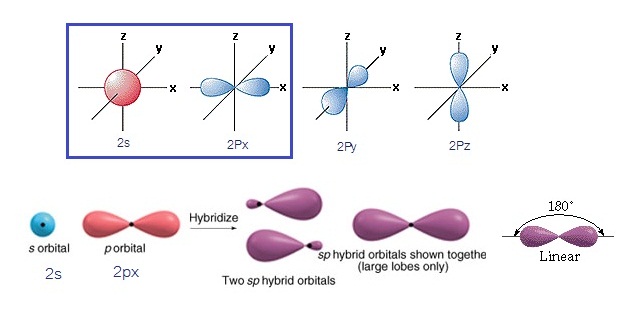
(ЄХдщЁ ЊСрЁдДфЮКУдфДрЋЊбЙ sp ЂЭЇЄвУьКЭЙ)
фЮКУдДЭЭУьКдЗбХ sp2 рЁдДЂжщЙЈвЁЁвУУЧСЕбЧУаЫЧшвЇ
orbital 2s ЁбК orbital 2px сХа 2py фЮКУдДЭЭУьКдЗбХЗешрЁдДЂжщЙСеУйЛУшвЇрЛчЙЪвСрЫХешТСсКЙУвК
(Trigonal plana) ДбЇУйЛ

(ЄХдщЁ ЊСЁвУрЁдДфЮКУдфДрЋЊбЙ sp2
ЂЭЇЄвУьКЭЙ)
фЮКУдДЭЭУьКдЗбХ sp3 рЁдДЂжщЙЈвЁЁвУУЧСЕбЧУаЫЧшвЇ orbital 2s ЁбК orbital 2px 2py сХа pz фЮКУдДЭЭУьКдЗбХЗешрЁдДЂжщЙСеУйЛУшвЇрЛчЙЗУЇрЫХешТЙЪешЫЙщв (Tetrehedral)
ДбЇУйЛ
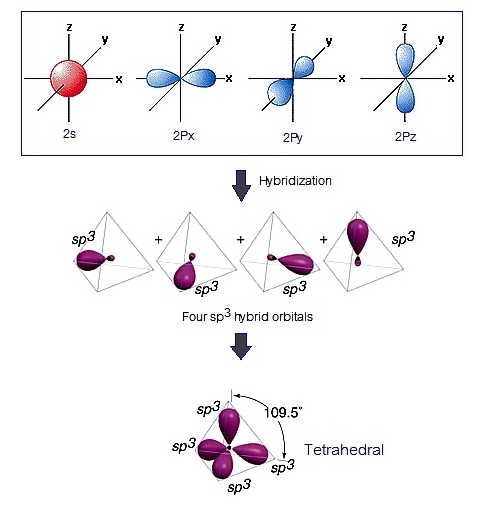
(ЄХдщЁ
ЊСЁвУрЁдДфЮКУдфДрЋЊбЙ
sp3 ЂЭЇЄвУьКЭЙ)
(ЄХдщЁ ЊСфЮКУдфДрЋЊбЙсХаУйЛЗУЇрУЂвЄГдЕЂЭЇфЮКУдДЭЭУьКдЗбХсККЕшвЇ
ц)
фЮКУдДЭЭУьКдЗбХЗбщЇ 3 сККДбЇЁХшвЧСвЙещ
рСзшЭЭаЕЭСЂЭЇЄвУьКЭЙЭТйшуЙЪвУЛУаЁЭКфЮтДУЄвУьКЭЙЗештСрХЁиХЛУаЁЭКДщЧТ C 2
ЭаЕЭС рЊшЙ C2H6 C2H4 сХа C2H2 ОбЙИаУаЫЧшвЇЭаЕЭСЂЭЇ C ЁбК
C ЈасЕЁЕшвЇЁбЙЄзЭ
* уЙ C2H6 ОбЙИаУаЫЧшвЇ C ЁбК
C рЛчЙОбЙИарДешТЧЊЙдД sigma bond ДбЇУйЛ
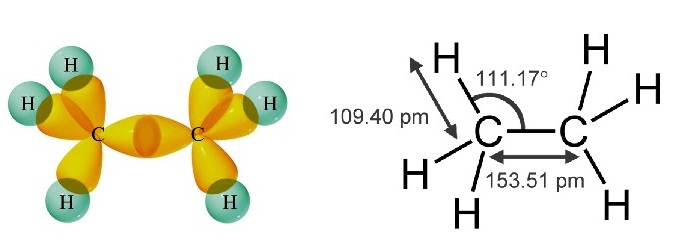
(ЄХдщЁ
ЊСЁвУрЁдД sigma bond уЙ C2H6 )
* уЙ C2H4 ОбЙИаУаЫЧшвЇ C ЁбК
C рЛчЙОбЙИарЛчЙОбЙИаЄйш ЛУаЁЭКДщЧТ sigma bond 1 ОбЙИа pi
bond 1 ОбЙИа ДбЇУйЛ

(ЄХдщЁ ЊСЁвУрЁдД sigma bond
сХа pi bond уЙ C2H4)
* уЙ C2H2 ОбЙИаУаЫЧшвЇ C ЁбК
C рЛчЙОбЙИаЪвС ЛУаЁЭКДщЧТ sigma bond
1 ОбЙИа
pi bond 2 ОбЙИа ДбЇУйЛ

(ЄХдщЁ ЊСЁвУрЁдД sigma bond
сХа pi bond уЙ C2H2)
*** ЪбЇрЁЕЄЧвСТвЧОбЙИа C-C > C=C > C C ДбЇУйЛ
ЁвУрЂеТЙЪйЕУХдЧЭдЪЂЭЇЪвУтЄрЧрХЙЕь
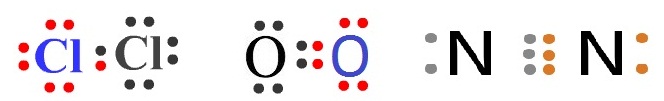
ЁвУрЂеТЙЪйЕУсЪДЇЁвУЪУщвЇОбЙИатЄрЧрХЙЕьУаЫЧшвЇЭаЕЭСЂЭЇИвЕирДеТЧЁбЙЈафСшТишЇТвЁ рОУвасЕшХаЭаЕЭССетЄУЇЪУщвЇрЫСзЭЙЁбЙ ЈгЙЧЙЭдрХчЁЕУЭЙЗешЕщЭЇЁвУрОдшСрОзшЭуЫщрЛчЙфЛЕвСЁЎЭЭЁрЕЕЈжЇСеЈгЙЧЙрЗшвЁбЙ ЉаЙбщЙсЕшХаЭаЕЭСЈауЊщрЧрХЙЋьЭдрХчЁЕУЭЙЈгЙЧЙрЗшвЁбЙСвЪУщвЇОбЙИаЁбЙ ЈауЊщЭдрХчЁЕУЭЙЭаЕЭСХаЁешЕбЧЁчЂжщЙЭТйшЁбКсЕшХаИвЕи ЧшвЕщЭЇЁвУЭдрХчЁЕУЭЙЭеЁЁешЕбЧЈжЇЄУК 8 уЊщЫХбЁЁвУЇшвТ ц ЧшвсЕшХаЭаЕЭСЈауЊщрЧрХЙЋьЭдрХчЁЕУЭЙрЗшвЁбКЈгЙЧЙЗешЕщЭЇЁвУрОзшЭуЫщЄУК 8 УшЧСЁбКЭаЕЭСЭзшЙ рЊшЙ ЁУГеЂЭЇ Cl2 O2 сХа N2
ЗешсЪДЇрЛчЙЕбЧЭТшвЇСвсХщЧ
Cl , O сХа N ЕщЭЇЁвУЭдрХчЁЕУЭЙрОдшСЭаЕЭСХа
1 , 2 сХа 3
ЕбЧ ЕвСХгДбК ЉаЙбщЙсЕшХаЭаЕЭСЈжЇуЊщрЧрХЙЋьЭдрХчЁЕУЭЙУшЧСЁбКЭаЕЭСЭзшЙЈгЙЧЙ 1 , 2 сХа 3
ЕбЧ рЛчЙЁвУуЊщЭдрХчЁЕУЭЙУшЧСЁбЙ 1
2 сХа 3
Єйш ЈжЇфДщОбЙИарДешТЧ ОбЙИаЄйш
сХаОбЙИаЪвС ЕвСХгДбК ДбЇУйЛ
сЕшЖщврЛчЙЁУГеЗешрЁдДЈвЁИвЕиЕшвЇЊЙдДСвЪУщвЇОбЙИаЁбЙ
ЖщвсЕшХаИвЕиСеЈгЙЧЙрЧрХЙЋьЭдрХчЁЕУЭЙрЗшвЁбЙ
ЁвУЪУщвЇОбЙИаЁчЈарЛчЙЗгЙЭЇрДеТЧЁбКЭаЕЭСЂЭЇИвЕирДеТЧЁбЙЪУщвЇОбЙИаЁбЙ
сЕшКвЇЄУбщЇЭвЈСеХбЁЩГаОдрШЩрОдшСЂжщЙКщвЇрЊшЙ ClF СерЧрХЙЋьЭдрХчЁЕУЭЙ = 7 рЫСзЭЙЁбЙ SO2 СерЧрХЙЋьЭдрХчЁЕУЭЙ = 6 рЫСзЭЙЁбЙ ЁвУЪУщвЇОбЙИарЛчЙДбЇУйЛ
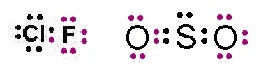
сЕшЖщвИвЕиСерЧрХЙЋьЭдрХчЁЕУЭЙфСшрЗшвЁбЙ ЁвУЪУщвЇОбЙИаЁчЈаСеЄЧвСЋбКЋщЭЙЂжщЙсЕшТбЇЄЇуЊщЫХбЁЁвУрДдС ЄзЭ сЕшХаЭаЕЭСЈауЊщрЧрХЙЋьЭдрХчЁЕУЭЙрЗшвЁбКЈгЙЧЙЗешЕщЭЇЁвУуЫщЄУК 8
уЙЁвУЪУщвЇОбЙИаЁбКЭаЕЭСЭзшЙ ЭвЈрЛчЙЁвУЪУщвЇОбЙИарДешТЧ ОбЙИаЄйшЫУзЭОбЙИаЪвС ЂжщЙЭТйшЁбКЁвУЈбДЭдрХчЁЕУЭЙЂЭЇсЕшХаИвЕи ЕщЭЇОдЈвУГврЛчЙУвТЁУГефЛ сЕшрОзшЭуЫщрЛчЙсЙЧЗвЇуЙЁвУрЂеТЙЪйЕУуЫщЖйЁЕщЭЇ ЄЧУОдЈвУГвЁЎ
5 ЂщЭ ДбЇЕшЭфЛЙещ
Lewis (Electron) Dot Formulas – 5
Easy Rules (ЁЎЇшвТ ц 5
ЂщЭЪгЫУбКЁвУрЂеТЙЪйЕУХдЧЭдЪ)
1. Determine Arrangement – Place the least electronegative
atom in the center. The halogens and
hydrogen
can never be in the center.
(ЈбДуЫщЭаЕЭСЗешСеЄшв EN ЕшгЗешЪиДрЛчЙЭаЕЭСЁХвЇ
ТЁрЧщЙИвЕиЮвтХрЈЙсХафЮтДУрЈЙрЛчЙЭаЕЭСЁХвЇфСшфДщ)
2. Determine total number of valence electrons. Two electrons are represented by one dash.
(add for negative ions, subtract for positive ions)
(ОдЈвУГвЈгЙЧЙрЧрХЙЋьЭдрХчЁЕУЭЙЗбщЇЫСДЂЭЇЗиЁЭаЕЭСЧшвСерЗшвфУ сХаЭдрХчЁЕУЭЙ 1
Єйш ЈарЂеТЙсЗЙДщЧТЂеД 1
ЂеДЁчфДщ ЖщврЛчЙфЭЭЭЙХКЈаСеЭдрХчЁЕУЭЙрОдшСЂжщЙЕвСЈгЙЧЙЂЭЇЛУаЈиХК уЙЂГаЗешфЭЭЭЙКЧЁЈаСеЈгЙЧЙ
ЭдрХчЁЕУЭЙХДХЇЕвСЈгЙЧЙЂЭЇЛУаЈиКЧЁ)
3. Attach central atom
to surrounding atoms. Molecule should be
symmetrical.
(ЭаЕЭСЭзшЙ ц
ЗешХщЭСУЭКЭаЕЭСЁХвЇЕщЭЇЭТйшуЙЕгсЫЙшЇЗешЪССвЕУ)
4. Distribute remaining electrons.
(уЪшЈиДсЪДЇЭдрХчЁЕУЭЙуЙЕгсЫЙшЇЕшвЇ ц
ЭТшвЇрЫСваЪС)
5. Use double or triple bonds if necessary. Hydrogen and the
halogens can never have a double or
triple
bond.
(ЈауЊщОбЙИаЄйшЫУзЭОбЙИаЪвСЕвСЄЧвСЈгрЛчЙ
сЕшЕщЭЇЗУвКЧшвЪгЫУбКИвЕифЮтДУрЈЙсХаЮвтХрЈЙЕшвЇ ц ЈаЪУщвЇОбЙ
ЄйшЫУзЭОбЙИаЪвСфСшфДщ)
рОдшСрЕдС
***
ЪдшЇЗешЗгуЫщрЁдДЄЧвСМдДОХвДфДщЇшвТуЙЁвУрЂеТЙЪйЕУХдЧЭдЪ ЂЭЇтСрХЁиХЗешЛУаЁЭКЭаЕЭСЕбщЇсЕш 3
ЭаЕЭСЂжщЙфЛЁчЄзЭ
фСшУйщЧшвЈауЊщЭаЕЭСЂЭЇИвЕиуДрЛчЙЭаЕЭСЁХвЇ
сЙаЙгЧшвуЫщуЊщЭаЕЭСЗешСерЧрХЙЋьЭдрХчЁЕУЭЙЙщЭТЗешЪиД ЫУзЭСеЄшв EN ЙщЭТЧшвИвЕиЭзшЙ ц рЛчЙЭаЕЭСЁХвЇ
ЭаЕЭСЗешСерЧрХЙЋьЭдрХчЁЕУЭЙСвЁЁЧшврЛчЙЭаЕЭСЗешХщЭСУЭКЭаЕЭСЁХвЇ
***
ЁвУОдЈвУГвЧшвЈауЊщЭдрХчЁЕУЭЙУшЧСЁбЙЁешЄйш уЫщДйЗешЭаЕЭСЗешСерЧрХЙЋьЭдрХчЁЕУЭЙСвЁЁЧшв
ЋжшЇЁчЄзЭЭаЕЭСЗешХщЭСУЭКЭаЕЭСЁХвЇсЕшХаЭаЕЭС ЧшвЂвДЭдрХчЁЕУЭЙЁешЕбЧЈжЇЈаЄУК 8
ЈауЊщЭдрХчЁЕУЭЙЕвСЈгЙЧЙЗешТбЇЂвДУшЧСЁбКЭаЕЭСЁХвЇ ЖщвЂвД
1 ЕбЧ ЈауЊщЭдрХчЁЕУЭЙУшЧСЁбЙ 1
Єйш ЪУщвЇОбЙИарДешТЧ ЖщвЂвД
2 ЕбЧ ЈауЊщЭдрХчЁЕУЭЙУшЧСЁбЙ 2 Єйш ЪУщвЇОбЙИаЄйш ЖщвЂвД
3 ЕбЧ ЈауЊщЭдрХчЁЕУЭЙУшЧСЁбЙ 3
Єйш ЪУщвЇОбЙИаЪвС
***
ЪдшЇЗешМдДОХвДКшЭТЭеЁрУзшЭЇЫЙжшЇЄзЭ
ЈгЙЧЙЈиДЗешуЊщсЪДЇЈгЙЧЙЭдрХчЁЕУЭЙфСшЕУЇЁбКЄЧвСрЛчЙЈУдЇ рОзшЭЛщЭЇЁбЙЄЧвСМдДОХвД
уЫщЙбКЈгЙЧЙрЧрХЙЋьЭдрХчЁЕУЭЙЂЭЇЗиЁИвЕиуЙтСрХЁиХЧшвСерЗшвфУ ЈгЙЧЙЈиДЕщЭЇСерЗшвЁбЙ ЖщвСвЁЁЧшвЫУзЭЙщЭТЁЧшвЈаМдД
(ЄХдщЁ ЊСЕбЧЭТшвЇЁвУЪУщвЇОбЙИатЄрЧрХЙЕь)
(ЄХдщЁ ЊСЁвУЪУщвЇОбЙИаУаЫЧшвЇЭаЕЭСЂЭЇИвЕиЕшвЇ
ц)
(ЄХдщЁ ЊСсХаЭшвЙЄгЭИдКвТЁвУрЂеТЙЪйЕУХдЧЭдЪ)
ЕбЧЭТшвЇ ЈЇрЂеТЙЪйЕУХдЧЭдЪЂЭЇ OCl2
ЧдИеЗг 17Cl ЁбК 8O
СеЁвУЈбДЭдрХчЁЕУЭЙДбЇЙещ
17Cl 2
8 7 СерЧрХЙЋьЭдрХчЁЕУЭЙ 7
ЕщЭЇЁвУЭеЁ 1 рОзшЭуЫщЄУК 8 ЈжЇЪУщвЇОбЙИарДешТЧфДщЭТшвЇрДеТЧ
8O
2 6 СерЧрХЙЋьЭдрХчЁЕУЭЙ 6
ЕщЭЇЁвУЭеЁЭеЁ 2 рОзшЭуЫщЄУК 8
ЈжЇЕщЭЇЪУщвЇОбЙИарДешТЧЁбК Cl
2 ЭаЕЭС ДбЇУйЛ

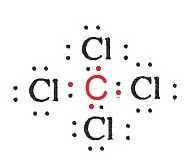
ЕбЧЭТшвЇ ЈЇрЂеТЙЪйЕУХдЧЭдЪЂЭЇ CCl4
ЧдИеЗг 6C ЁбК 17Cl СеЁвУЈбДЭдрХчЁЕУЭЙДбЇЙещ
17Cl 2 8
7 СерЧрХЙЋьЭдрХчЁЕУЭЙ 7 ЕщЭЇЁвУЭеЁ 1 ЈжЇЈаЄУК
8 ЪУщвЇОбЙИарДешТЧфДщЭТшвЇрДеТЧ
6C 2 4 СерЧрХЙЋьЭдрХчЁЕУЭЙ 4
ЕщЭЇЁвУЭеЁ 4 рОзшЭуЫщЄУК
8 ЕщЭЇЪУщвЇОбЙИарДешТЧЁбК Cl 4
ЭаЕЭС
ДбЇУйЛ
ЕбЧЭТшвЇ ЈЇрЂеТЙЪйЕУХдЧЭдЪЂЭЇ CO2
ЧдИеЗг 6C ЁбК 8O ЈбДЭдрХчЁЕУЭЙДбЇЙещ
8O 2
6 СерЧрХЙЋьЭдрХчЁЕУЭЙ 6
ЕщЭЇЁвУЭеЁ 2 ЈжЇЈаЄУК 8 ЈжЇЪУщвЇЄйш 1
ОбЙИаЁбК C
6C
2 4 СерЧрХЙЋьЭдрХчЁЕУЭЙ
4 ЕщЭЇЁвУЭеЁ 4 ЈжЇЈаЄУК 8
ЈжЇЕщЭЇЪУщвЇОбЙИаЄйшЁбК O 2 ЭаЕЭС
ЭаЕЭСХа 1 ОбЙИа ДбЇУйЛ
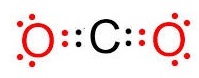
ЕбЧЭТшвЇ ЈЇрЂеТЙЪйЕУХдЧЭдЪЂЭЇ CO
ЧдИеЗг 6C ЁбК 8O ЈбДЭдрХчЁЕУЭЙДбЇЙещ
8O 2
6 СерЧрХЙЋьЭдрХчЁЕУЭЙ 6
ЕщЭЇЁвУЭеЁ 2 ЈжЇЈаЄУК 8
уЊщЭдрХчЁЕУЭЙУшЧСЁбК O 2 ЕбЧ
6C
2 4 СерЧрХЙЋьЭдрХчЁЕУЭЙ
4 ЕщЭЇЁвУЭеЁ 4
ЈжЇЈаЄУК 8 ЁвУЪУщвЇОбЙИаЈарЛчЙ ДбЇУйЛ

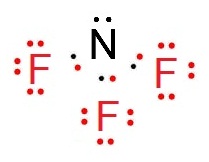
ЕбЧЭТшвЇ ЈЇрЂеТЙЪйЕУХдЧЭдЪЂЭЇ NF3
ЧдИеЗг
9F ЁбК 7N
ЈбДЭдрХчЁЕУЭЙДбЇЙещ
9F 2
7 СерЧрХЙЋьЭдрХчЁЕУЭЙ 7 ЕщЭЇЁвУЭеЁ 1
ЈжЇЈаЄУК 8 ЈжЇЪУщвЇОбЙИарДешТЧЁбК N 1 ОбЙИа
7N 2
5 СерЧрХЙЋьЭдрХчЁЕУЭЙ 5 ЕщЭЇЁвУЭеЁ 3 ЈжЇЈаЄУК
8 ЈжЇЪУщвЇОбЙИарДешТЧЁбК F
3 ЭаЕЭС
ДбЇУйЛ
ОбЙИауЙфЭЭЭЙЗешрЛчЙЁХишСЭаЕЭС (bond in polyatomic ion)
фЭЭЭЙЗешрЛчЙЁХишСЭаЕЭС рЊшЙ NO3- CO32- SO42- PO43- … ЈгЙЧЙЛУаЈиХКрЁдДЈвЁЁвУСеЭдрХчЁЕУЭЙСвЁЁЧшвЛЁЕд
СеЛУаЈиХКрЗшвфУЁчЫСвТЄЧвСЧшвСеЭдрХчЁЕУЭЙСвЁЁЧшвЛЁЕдЭТйшЈгЙЧЙрЗшвЙбщЙ тДТЗбшЧфЛсХщЧЭдрХчЁЕУЭЙЗешСеСвЁЁЧшвЛЁЕдЙещЈаЭТйшЗешЭаЕЭСЁХвЇ
(ЭаЕЭСЗешЂеДрЪщЙуЕщ)
ЁвУЪУщвЇОбЙИаЈарЛчЙДбЇЙещ
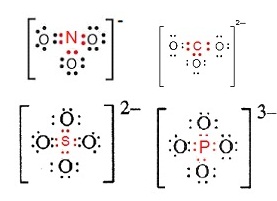
ЈвЁУйЛ ЖщвЪбЇрЁЕЈарЫчЙЧшв ...
рЧрХЙЋьЭдрХчЁЕУЭЙЂЭЇ N
рОдшСЈвЁ 5 рЛчЙ
6 ЄзЭСеЭдрХчЁЕУЭЙрОдшС 1
ЕбЧ ЕвСЛУаЈи 1-
рЧрХЙЋьЭдрХчЁЕУЭЙЂЭЇ C
рОдшСЈвЁ 4 рЛчЙ 6 ЄзЭСеЭдрХчЁЕУЭЙрОдшС 2
ЕбЧ ЕвСЛУаЈи 2-
рЧрХЙЋьЭдрХчЁЕУЭЙЂЭЇ S рОдшСЈвЁ 6 рЛчЙ
8 ЄзЭСеЭдрХчЁЕУЭЙрОдшС 2
ЕбЧ ЕвСЛУаЈи 2-
рЧрХЙЋьЭдрХчЁЕУЭЙЂЭЇ P рОдшСЈвЁ 5 рЛчЙ
8 ЄзЭСеЭдрХчЁЕУЭЙрОдшС 3
ЕбЧ ЕвСЛУаЈи 3-
рОдшСрЕдС
1. ЭаЕЭСЂЭЇ H сХаИвЕиЮвтХрЈЙЈаЪУщвЇОбЙИарДешТЧЁбКЭаЕЭСЭзшЙ
ц рЪСЭ сХарЛчЙЭаЕЭСЁХвЇЂЭЇ
тСрХЁиХфСшфДщ
2. ИвЕиЮвтХрЈЙЈаЪУщвЇОбЙИарДешТЧфДщЭТшвЇрДеТЧ
фСшЧшвЈаЪУщвЇОбЙИаЁбКИвЕирДеТЧЁбЙЫУзЭИвЕиЕшвЇЊЙдДЁбЙ
рЊшЙ F-F Cl-Cl
Br-Br I-I Cl-F
Br-Cl Br-I
3. ЖщвЭаЕЭССерЧрХЙЋьЭдрХчЁЕУЭЙ
= 6
3.1
ЪУщвЇОбЙИаЁбКЭаЕЭСЗешСерЧрХЙЋьЭдрХчЁЕУЭЙ = 6 рЊшЙЁбЙ
ЈаЪУщвЇОбЙИаЄйш рЊшЙ O=O
3.2 ЪУщвЇОбЙИаЁбК H ЫУзЭИвЕиЗешСерЧрХЙЋьЭдрХчЁЕУЭЙ = 7 ЈаЪУщвЇОбЙИарДешТЧ 2 ОбЙИа
рЊшЙ H2O
Cl2O
4. ЖщвЭаЕЭССерЧрХЙЋьЭдрХчЁЕУЭЙ
= 5
3.1 ЪУщвЇОбЙИаЁбКЭаЕЭСЗешСерЧрХЙЋьЭдрХчЁЕУЭЙ
= 5 рЊшЙЁбЙ ЈаЪУщвЇОбЙИаЪвС рЊшЙ
3.2 ЪУщвЇОбЙИаЁбК H ЫУзЭИвЕиЗешСерЧрХЙЋьЭдрХчЁЕУЭЙ
= 7 ЈаЪУщвЇОбЙИарДешТЧ 3 ОбЙИа рЊшЙ NH3
PCl3
5. СеЂщЭТЁрЧщЙЕшвЇ ц ЭТйшКщвЇЗешЈаЁХшвЧЖжЇуЙЕЭЙЕшЭ ц фЛ
ЁвУрЂеТЙЪйЕУсХаЁвУрУеТЁЊзшЭЪвУтЄрЧрХЙЕь
рУвСбЁЈаЄищЙрЄТЁбКЁвУрЂеТЙЪйЕУЂЭЇЪвУтЄрЧрХЙЕьЕвСЗешОКрЫчЙ рЊшЙ рЂеТЙЧшв
H2O ЫСвТЖжЇЙщг
сЕшфСшрЂеТЙЧшв OH2 (ТЁрЧщЙуЙЁвУрЂеТЙсЪДЇЪйЕУсЪДЇтЄУЇЪУщвЇЂЭЇтСрХЁиХЗешЋбКЋщЭЙрОзшЭсЪДЇуЫщрЫчЙЧшвтСрХЁиХЫбЙДщвЙуДрЂщвЫвЁбЙ) уЙЁвУрЂеТЙЪйЕУтСрХЁиХЂЭЇЪвУтЄрЧрХЙЕьЙбщЙЈарУеТЇХгДбКЂЭЇИвЕиЭТшвЇфУ СеЫХбЁЁвУЁвУЁЧщвЇ ц ЧшвуЫщДйЕгсЫЙшЇЂЭЇИвЕиуЙЕвУвЇИвЕи уЫщрЂеТЙЪбХбЁЩГьЂЭЇИвЕиЗешЭТйшДщвЙЋщвТЂЭЇЕвУвЇИвЕиЁшЭЙ сХщЧЈжЇЕвСДщЧТИвЕиЗешЭТйшЗвЇЂЧвЕшЭрЙзшЭЇЁбЙфЛ (ЄХдщЁ ДйЕвУвЇИвЕи)
рЊшЙ
HCl HNO3 PCl3 CCl4 сЕшЫХбЁЁвУЙещуЊщЁбКЪвУЗбщЇЫСДфСшфДщ
рОУваСеКвЇЊЙдДЗешрЂеТЙИвЕиЗешЭТйшЗвЇЂЧвЁшЭЙИвЕиЗвЇЋщвТ рЊшЙ NH3 HClO3 ЈжЇСеЂщЭЁгЫЙДуЙЁвУрУеТЇХгДбКЂЭЇИвЕиЁшЭЙ-ЫХбЇДбЇЙещ
B
, Si , C , P , H , S , I , Br , Cl , O сХа F.
ХгДбКЁшЭЙЫУзЭЫХбЇЂЭЇИвЕиуЙЪйЕУЂЭЇЁвУЛУаЁЭК СеМХЕшЭЁвУрУеТЁЊзшЭЂЭЇЪвУЙбщЙ ц рОУваЁвУрУеТЁЊзшЭЈарУеТЁЕвСХгДбКЂЭЇИвЕиЗешсЪДЇЭТйшуЙЪйЕУЂЭЇЪвУ (ТЁрЧщЙЁУГеЗешрУеТЁДщЧТЊзшЭЪвСб) рЊшЙ HCl рУеТЁЊзшЭЧшв фЮтДУрЈЙЄХЭфУДь ЖщврЂеТЙЪйЕУрЛчЙ ClH ЈаЕщЭЇрУеТЁЧшв ЄХЭУеЙфЮфДУДь
ЉаЙбщЙЁвУЁгЫЙДХгДбКЂЭЇИвЕиуЙЁвУрЂеТЙЪйЕУЂЭЇЪвУтЄрЧрХЙЕь ЈжЇрЛчЙМХДеуЙЁвУЛщЭЇЁбЙЄЧвСЪбКЪЙЂЭЇЁвУрУеТЁЊзшЭЪвУрДеТЧЁбЙ
ЁвУрУеТЁЊзшЭЪвУтЄрЧрХЙЕьЈжЇСеЄЧвСТишЇТвЁЁЧшвЁвУрУеТЁЊзшЭЪвУфЭЭЭЙдЁ КвЇЊЙдДуЊщЊзшЭЪвСб (common names ) рЊшЙ CH4 рУеТЁЧшв methane
NH3 рУеТЁЧшв ammonia
H2O
рУеТЁЧшв water сЕшЭТшвЇфУЁчЕвССеЫХбЁЁвУЗбшЧфЛЂЭЇЁвУрУеТЁЊзшЭДбЇЙещ
1. рУдшСЕщЙДщЧТЊзшЭЂЭЇИвЕиЕбЧсУЁЗешсЪДЇЭТйшуЙЪйЕУЂЭЇЪвУЛУаЁЭК сХаЖщвСеЈгЙЧЙЭаЕЭССвЁЁЧшв 1
ЕщЭЇКЭЁЈгЙЧЙЭаЕЭСДщЧТРвЩвХаЕдЙ ( 1 = mono, 2 = di-, 3 = tri-, 4 = tetra-, 5 = penta-,6
= hexa-, 8 = octa- , 9 = nona- , 10 =
deca-)
2. ЄгХЇЗщвТЈарЛчЙЊзшЭЂЭЇИвЕиЗешЭТйшЗщвТуЙЪйЕУЂЭЇЪвУЛУаЁЭК сЕшуЫщрЛХешТЙрЪеТЇЄгХЇЗщвТрЛчЙЪгрЙеТЇ
–ide ЄгЧшв mono ЈафСшуЊщуЙЁвУрУеТЁЊзшЭЪвУЗбшЧ ц
фЛ
сЕшЈауЊщЪгЫУбКЪвУЛУаЁЭКЭЭЁфЋДьрЗшвЙбщЙ
3. ЖщвИвЕиЗешЭТйшЗщвТрЛчЙ polyatomic ion рЊшЙ CN- , фЋТвфЙДь
рЪеТЇЄгЗщвТЈауЊщЊзшЭЂЭЇфЭЭЭЙЙбщЙ
ЕбЧЭТшвЇ
|
ЪвУЕбЧЭТшвЇ
|
ЁвУрУеТЁЊзшЭ
|
|
NO2
|
фЙтЕУрЈЙфДЭЭЁфЋДь
|
|
N2O
|
фДфЙтЕУрЈЙЭЭЁфЋДь
|
|
N2O4
|
фДфЙтЕУрЈЙрЕЕУаЭЭЁфЋДь
|
|
PCl3
|
ПЭЪПЭУбЪфЕУЄХЭфУДь
|
|
PCl5
|
ПЭЪПЭУбЪрОЙЕаЄХЭфУДь
|
|
CO
|
ЄвУьКЭЙтСтСЭЭЁфЋДь(ЄвУьКЭЙСЭЙЭЁфЋДь)
|
|
CO2
|
ЄвУьКЭЙфДЭЭЁфЋДь
|
|
HCN
|
фЮтДУрЈЙфЋТвфЙДь
|
сККНжЁЫбД
1. ЈЇрЂеТЙЪйЕУХдЧЭдЪ (Lewis Diagrams
, Lewis structure,
Lewis
electron-dot structure) ЗбщЇсККрЕчСсХасККТшЭ
рОзшЭсЪДЇЁвУЪУщвЇОбЙИаЂЭЇЪвУЕшЭфЛЙещсХарУеТЁЊзшЭЪвУДбЇЁХшвЧДщЧТ
|
ЪвУ
|
ЪйЕУсККрЕчС
|
ЪйЕУсККТшЭсЪДЇЭдрХчЁЕУЭЙЄйштДДрДешТЧ
|
ЪйЕУсККТшЭфСшсЪДЇЭдрХчЁЕУЭЙЄйштДДрДешТЧ
|
ЊзшЭЪвУ
|
|
H2O
|
|
|
|
water ,Йщг
(common name,
ЊзшЭЪвСб)
|
|
CO2
|
|
|
|
|
|
HCN
|
|
|
|
|
|
C2H5OH
|
|
|
|
|
|
CH4
|
|
|
|
|
|
C2H6
|
|
|
|
|
|
C2H4
|
|
|
|
|
|
C2H2
|
|
|
|
|
|
CH3COOH
|
|
|
|
|
|
PH3
|
|
|
|
|
|
NCl3
|
|
|
|
|
|
CH2O
|
|
|
|
|
|
CCl4
|
|
|
|
|
|
CS2
|
|
|
|
|
2.
Which of the following is the correct formula for a compound of carbon and
chlorine?
(ЪйЕУЂЭЇЪвУЛУаЁЭКУаЫЧшвЇЄвУьКЭЙЁбКЄХЭУеЙЂщЭуДЖйЁЕщЭЇ)
a) CCl b) CCl4 c) CCl3 d) C2Cl e) C3Cl2
3. Double bonds in molecules: (ОбЙИаЄйш
СеЄЧвСЫСвТЕУЇЁбКЂщЭуД)
a) occur
in atoms having two valence electrons. (рЁдДЂжщЙЁбКЭаЕЭСЗешСерЧрХЙЋьЭдрХчЁЕУЭЙрЗшвЁбК
2)
b) involve sharing two electrons.
(уЊщЭдрХчЁЕУЭЙУшЧСЁбЙ
2 ЕбЧ)
c) must
be ionic. (рЛчЙЪвУфЭЭЭЙдЁ)
d)
involve sharing four electrons. (уЊщЭдрХчЁЕУЭЙУшЧСЁбЙ
4 ЕбЧ)
e) occur in polyatomic ions. (ЕщЭЇЭТйшуЙфЭЭЭЙЗешрЛчЙЁХишСЭаЕЭС)
3. Consider the following elements and select the one which has the largest
number of electrons shown in an
electron dot symbol. Cl
Mg Ga S Si
(ЈЇОдЈвУГвЧшвИвЕиуДЕшЭфЛЙещрСзшЭрЂеТЙЪйЕУсЪДЇЭдрХчЁЕУЭЙДщЧТЈиДсХщЧ ИвЕиуДСеЈиДСвЁЗешЪиД)
a) Mg b) Cl c) Ga d) Si e) S
4. Which
of the following is an acceptable Lewis structure for NH2NH2? (Ans.III) (тЄУЇЪУщвЇсККХдЧЭдЪЂЭЇ
NH2NH2 ЗешТЭСУбКфДщ рЛчЙДбЇЂщЭуД)

5.
Which of the following is an acceptable
Lewis structure for HOOH? (Ans.III) (тЄУЇЪУщвЇсККХдЧЭдЪЂЭЇ
HOOH ЗешТЭСУбКфДщрЛчЙ ДбЇЂщЭуД)
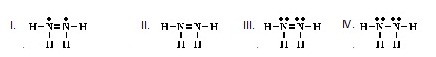
6. Which of the following is an acceptable Lewis
structure for CH3SH?
(Ans.III) (тЄУЇЪУщвЇсККХдЧЭдЪЂЭЇ
CH3SH ЗешТЭСУбКфДщрЛчЙДбЇЂщЭуД)
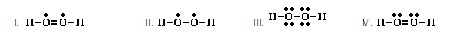
7. Which of the following is the correct Lewis
structure for CS2? (Ans.V) (тЄУЇЪУщвЇсККХдЧЭдЪЂЭЇ CS2 ЗешТЭСУбК
фДщрЛчЙДбЇЂщЭуД)
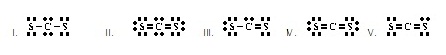
8.
Which of the
following is an acceptable Lewis structure for H2CO? (Ans.IV) (тЄУЇЪУщвЇсККХдЧЭдЪЂЭЇ H2CO
ЗешТЭСУбКфДщрЛчЙДбЇ ЂщЭуД)

9.
Which of the following is an acceptable Lewis structure for HNNH? (Ans.I) (тЄУЇЪУщвЇсККХдЧЭдЪЂЭЇ HNNH
ЗешТЭСУбКфДщрЛчЙДбЇЂщЭуД)
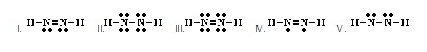
10.
Which of the
following is an acceptable Lewis structure for HCN? (Ans.III) (тЄУЇЪУщвЇсККХдЧЭдЪЂЭЇ HCN
ЗешТЭСУбКфДщрЛчЙДбЇЂщЭуД)
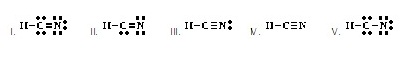
11. Which of the following is an acceptable Lewis
structure for C2H2? (Ans.IV) (тЄУЇЪУщвЇсККХдЧЭдЪЂЭЇ C2H2
ЗешТЭСУбКфДщрЛчЙДбЇЂщЭуД)
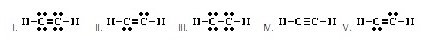
12. Which of the following is an acceptable Lewis
structure for CO? (Ans.II) (тЄУЇЪУщвЇсККХдЧЭдЪЂЭЇ CO Зеш
ТЭСУбКфДщрЛчЙДбЇЂщЭуД)
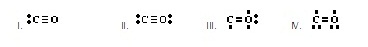
13.
Indicate the # of VALENCE electrons for
each species. Write the correct Lewis
electron-dot structure for each.
(ЈЇКЭЁЈгЙЧЙрЧрХЙЋьЭдрХчЁЕУЭЙЗбщЇЫСДЂЭЇЪвУсЕшХаЊЙдДЕвСЗешЗешЁгЫЙД сХарЂеТЙЪйЕУтЄУЇЪУщвЇХдЧЭдЪДщЧТ)

Content's Picture

Size : 32.31 KBs
Upload : 2014-08-07 22:02:56
|
|
 
Status : МйщуЊщЗбшЧфЛ
ЧдЗТвШвЪЕУь
|
|
|